Ензими
дефиниција
Ензими су хемијске супстанце које се могу наћи по целом телу. Покрећу хемијске реакције у телу.
историја
Реч ензим је направио Вилхелм Фриедрицх Кухне 1878 а изведено је из грчке израђене речи енцимон, што значи квасац или кисело тесто. Ово је онда нашло пут у међународну науку. Тхе међународна унија чисте примењене хемије (ИУПАЦ) и међународна унија биохемије (ИУБМБ) је развио номенклатуру за ензиме која представнике ове велике групе супстанци дефинише као заједничку групу. Именовање којим се ензими класификују према њиховим задацима важно је за одређивање задатака појединих ензима.
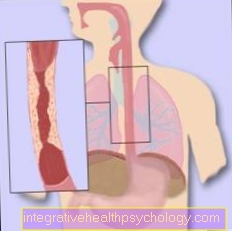
Илустрација ензима
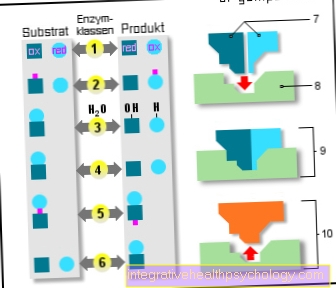
Ензими
6 класа ензима:
- Оксидоредуктазе
(Оксидација / редукција) - Трансферазе
(Преношење) - Хидролазе
(Употреба воде) - Лиасес
(Деколте) - Изомеразе
(иста емпиријска формула) - Лигасес
(Реакције сабирања) - Подлоге
- Активни центар
- Ензим / супстрат
комплекс - Ензим / производ
комплекс
Преглед свегаСлике Др-Гумперта можете наћи на: медицинске илустрације
Именовање
Тхе Именовање ензим је укључен три основна принципа заснован. Имена ензима који се завршавају на –аза описују неколико ензима у систему. Само име ензима описује реакцију коју ензим покреће (катализовано). Назив ензима је такође класификација ензима. Поред тога, кодни систем који ЕЦ систем бројева, у којој су ензими направљени под нумеричким кодом четири броја може се наћи. Први број означава класу ензима. Спискови свих откривених ензима осигуравају бржи проналазак наведеног ензимског кода. Иако су кодови засновани на својствима реакције коју ензим катализује, нумерички кодови се у пракси показују незграпни. Чешће се користе систематски називи засновани на горе наведеним правилима. Проблеми са номенклатуром настају, на пример, са ензимима који катализују неколико реакција. Стога понекад постоји неколико имена за њих. Неки ензими имају тривијална имена која не указују на то да је поменута супстанца ензим. Будући да су имена традиционално широко употребљавана, нека од њих су задржана.
Класификација према функцији ензима
Према ИУПАЦ и ИУБМБ, ензими су подељени у шест класа ензима према реакцији коју покрећу:
- Оксидоредуктазе
Оксидоредуктазе покрећу редокс реакције. У овој хемијској реакцији, електрони се преносе са једног реакционог партнера на другог. Једна супстанца ослобађа електроне (оксидација), а друга супстанца прима електроне (редукција).
Формула за катализовану реакцију је А ?? + Б? А? + Б?.
Супстанца А ослобађа електрон (?) И оксидује се, док супстанца Б апсорбује овај електрон и редукује се. Због тога се редокс реакције називају и реакцијама редукције-оксидације.
Многе метаболичке реакције су редокс реакције. Оксигеназе преносе један или више атома кисеоника на свој супстрат. - Трансферазе
Трансферазе преносе функционалну групу са једног супстрата на други. Функционалне групе су атомске групе у органским једињењима које у великој мери одређују особине супстанце и реакционо понашање. Хемијска једињења која имају исте функционалне групе груписана су у класе супстанци због сличних својстава. Функционалне групе биће подељене према томе да ли су хетероатоми или не. Хетероатоми су сви атоми у органским једињењима који нису ни угљеник ни водоник.
Нпр .: -ОХ -> хидроксилна група (алкохоли) - Хидролазе
Хидролазе раздвајају везе у реверзибилним реакцијама користећи воду. Естри, естри, пептиди, гликозиди, анхидриди киселина или везе Ц-Ц. Реакција равнотеже је: А-Б + Х2О? А-Х + Б-ОХ.
Ензим који припада групи хидролазе је нпр. Алфа галактозидаза. - Лиасес
Лиазе, такође називане синтазама, катализују цепање сложених производа од једноставних подлога без одвајања АТП-а. Шема реакције је А-Б → А + Б.
АТП је аденозин трифосфат и нуклеотид, који се састоји од трифосфата нуклеозида аденозина (и као такав енергетски богат градивни елемент РНК нуклеинске киселине). Међутим, АТП је углавном универзални облик одмах доступне енергије у свакој ћелији и истовремено важан регулатор процеса снабдевања енергијом. Ако је потребно, АТП се поново синтетише из других залиха енергије (креатин фосфат, гликоген, масне киселине). Молекул АТП састоји се од остатка аденина, шећерне рибозе и три фосфата (? До?) У естеру (?) Или анхидридним везама (? И?). - Изомеразе
Изомеразе убрзавају хемијску конверзију изомера. Изомерија је појава два или више хемијских једињења са потпуно истим атомима (исте емпиријске формуле) и молекулском тежином, која се, међутим, разликују у повезаности или просторном распореду атома. Одговарајућа једињења називају се изомери.
Ови изомери се разликују по хемијским и / или физичким, а често и по биохемијским својствима. Изомеризам се јавља првенствено код органских једињења, али и код (неорганских) координационих једињења. Изомерија је подељена на различита подручја. - Лигасес
Лигазе катализују стварање супстанци које су хемијски сложеније од супстрата који се користе, али су, за разлику од лиаза, само ензиматски ефикасне са цепањем АТП. За стварање ових супстанци потребна је енергија која се добија цепањем АТП-а.
Неки ензими су у стању да катализују неколико, понекад врло различитих реакција. Ако је то случај, они се додељују у неколико класа ензима.
Можда ће вас занимати и ови чланци:
- Алфа-глукозидаза
- Липаза
- Трипсин
Класификација према структури ензима
Готово сви ензими су протеини и могу се класификовати на основу дужине протеинског ланца:
- Мономери
Ензими који се састоје од само једног протеинског ланца - Олигомери
Ензими који се састоје од неколико протеинских ланаца (мономера) - Вишеензимски ланци
Неколико агрегираних ензима који међусобно сарађују и регулишу. Ови ланци ензима катализују узастопне кораке у метаболизму ћелије.
Поред тога, постоје појединачни ланци протеина који садрже неколико ензимских активности; они се називају мултифункционалним ензимима.
Класификација према кофакторима
Друга класификација је класификација према разматрању кофактора. Кофактори, коензими и ко-супстрати су називи за различите класификације супстанци које утичу на биохемијске реакције њиховом интеракцијом са ензимима.
У обзир се узимају органски молекули и јони (углавном јони метала).
Чисти протеински ензими састоје се искључиво од протеина, а активни центар се формира само од остатака аминокиселина и окоснице пептида. Аминокиселине су класа органских једињења са најмање једном карбокси групом (-ЦООХ) и једном амино групом (-НХ2).
Холоензими се састоје од протеинске компоненте, апоензима, и кофактора, молекула мале молекулске тежине (не протеина). Обе заједно су важне за функцију ензима.
Коензими
Органски молекули као кофактори називају се коензимима. Ако су ковалентно везани за апоензим, називају се протетске групе или ко-супстрати. Протетска група односи се на не-протеинске компоненте чврсто (углавном ковалентно) везане за протеин са каталитичким ефектом.
Козубстрати су називи за различите класификације супстанци које утичу на биохемијске реакције њиховом интеракцијом са ензимима. Као биокатализатори, молекули убрзавају реакције у организмима, ензими убрзавају биохемијске реакције. Смањују енергију активације коју треба савладати како би се супстанца могла претворити.